Mengkaji sifat-sifat gas ideal ialah topik penting dalam fizik. Pengenalan kepada ciri-ciri sistem gas bermula dengan pertimbangan persamaan Boyle-Mariotte, kerana ia adalah undang-undang pertama yang ditemui secara eksperimen bagi gas ideal. Mari pertimbangkan dengan lebih terperinci dalam artikel.
Apakah yang dimaksudkan dengan gas ideal?
Sebelum bercakap tentang undang-undang Boyle-Mariotte dan persamaan yang menerangkannya, mari kita takrifkan gas ideal. Ia lazimnya difahami sebagai bahan bendalir di mana zarah-zarah yang membentuknya tidak berinteraksi antara satu sama lain, dan saiznya amat kecil jika dibandingkan dengan purata jarak antara zarah.
Malah, sebarang gas adalah nyata, iaitu atom dan molekul konstituennya mempunyai saiz tertentu dan tidak berinteraksi antara satu sama lain dengan bantuan daya van der Waals. Walau bagaimanapun, pada suhu mutlak yang tinggi (lebih daripada 300 K) dan tekanan rendah (kurang daripada satu atmosfera), tenaga kinetik atom dan molekul jauh lebih tinggi daripada tenaga interaksi van der Waals, jadi gas sebenar pada yang ditunjukkankeadaan dengan ketepatan yang tinggi boleh dianggap ideal.
Persamaan Boyle-Mariotte
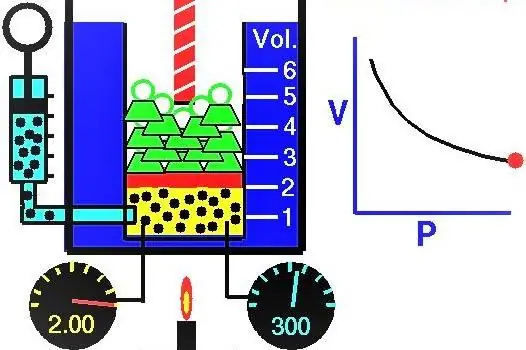
Sifat gas yang diterokai secara aktif oleh saintis Eropah pada abad XVII-XIX. Undang-undang gas pertama yang ditemui secara eksperimen ialah undang-undang yang menerangkan proses isoterma pengembangan dan pemampatan sistem gas. Eksperimen yang sepadan telah dijalankan oleh Robert Boyle pada tahun 1662 dan Edm Mariotte pada tahun 1676. Setiap saintis ini secara bebas menunjukkan bahawa semasa proses isoterma dalam sistem gas tertutup, tekanan berubah secara songsang dengan isipadu. Ungkapan matematik proses yang diperoleh secara eksperimen ditulis dalam bentuk berikut:
PV=k
Di mana P dan V ialah tekanan dalam sistem dan isipadunya, k ialah beberapa pemalar, yang nilainya bergantung kepada jumlah bahan gas dan suhunya. Jika anda membina pergantungan fungsi P(V) pada graf, maka ia akan menjadi hiperbola. Contoh lengkung ini ditunjukkan di bawah.
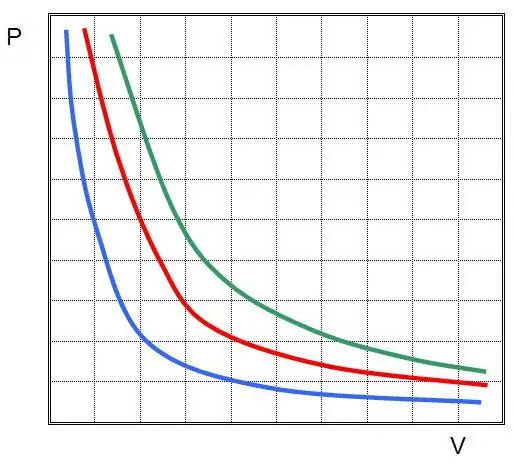
Persamaan bertulis dipanggil persamaan (undang-undang) Boyle-Mariotte. Undang-undang ini boleh dirumuskan secara ringkas seperti berikut: pengembangan gas ideal pada suhu malar membawa kepada penurunan berkadar dalam tekanan di dalamnya, sebaliknya, mampatan isoterma sistem gas disertai dengan peningkatan berkadar dalam tekanan di dalamnya.
Persamaan gas ideal
Undang-undang Boyle-Mariotte ialah kes khas undang-undang yang lebih umum yang mengandungi nama Mendeleev danClapeyron. Emile Clapeyron, meringkaskan maklumat eksperimen tentang kelakuan gas di bawah pelbagai keadaan luaran, pada tahun 1834 memperoleh persamaan berikut:
PV=nRT
Dengan kata lain, hasil darab isipadu V sistem gas dan tekanan P di dalamnya adalah berkadar terus dengan hasil darab suhu mutlak T dan jumlah bahan n. Pekali perkadaran ini dilambangkan dengan huruf R dan dipanggil pemalar sejagat gas. Dalam persamaan bertulis, nilai R muncul kerana penggantian beberapa pemalar, yang dibuat oleh Dmitry Ivanovich Mendeleev pada tahun 1874.
Dari persamaan keadaan universal adalah mudah untuk melihat bahawa kestabilan suhu dan jumlah bahan menjamin invarian bahagian kanan persamaan, yang bermaksud bahawa bahagian kiri persamaan juga akan kekal malar. Dalam kes ini, kita mendapat persamaan Boyle-Mariotte.

Undang-undang gas lain
Persamaan Clapeyron-Mendeleev yang ditulis dalam perenggan di atas mengandungi tiga parameter termodinamik: P, V dan T. Jika setiap daripada mereka tetap, dan dua yang lain dibenarkan untuk berubah, maka kita mendapat Boyle-Mariotte, Persamaan Charles dan Gay-Lussac. Undang-undang Charles bercakap tentang perkadaran langsung antara isipadu dan suhu untuk proses isobarik, dan undang-undang Gay-Lussac menyatakan bahawa dalam kes peralihan isokhorik, tekanan gas meningkat atau menurun dalam perkadaran langsung kepada suhu mutlak. Persamaan yang sepadan kelihatan seperti ini:
V/T=const apabila P=const;
P/T=const apabila V=const.
JadiOleh itu, undang-undang Boyle-Mariotte adalah salah satu daripada tiga undang-undang gas utama. Walau bagaimanapun, ia berbeza daripada yang lain dari segi pergantungan grafik: fungsi V(T) dan P(T) ialah garis lurus, fungsi P(V) ialah hiperbola.
Contoh tugas untuk menerapkan undang-undang Boyle-Mariotte
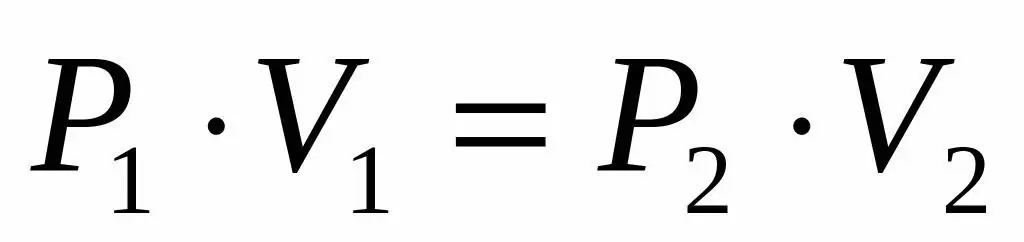
Isipadu gas dalam silinder di bawah omboh pada kedudukan awal ialah 2 liter, dan tekanannya ialah 1 atmosfera. Berapakah tekanan gas selepas omboh naik dan isipadu sistem gas meningkat sebanyak 0.5 liter. Proses ini dianggap seisoterma.
Memandangkan kita diberi tekanan dan isipadu gas ideal, dan kita juga tahu bahawa suhu kekal tidak berubah semasa pengembangannya, kita boleh menggunakan persamaan Boyle-Mariotte dalam bentuk berikut:
P1V1=P2V 2
Kesamaan ini mengatakan bahawa produk tekanan isipadu adalah malar untuk setiap keadaan gas pada suhu tertentu. Menyatakan nilai P2 daripada kesamaan, kami memperoleh formula akhir:
P2=P1V1/V 2
Apabila melakukan pengiraan tekanan, anda boleh menggunakan unit luar sistem dalam kes ini, kerana liter akan mengecut, dan kami mendapat tekanan P2dalam atmosfera. Menggantikan data daripada keadaan, kami sampai pada jawapan kepada soalan masalah: P2=0.8 atmosfera.






