Peralihan adiabatik antara dua keadaan dalam gas bukanlah salah satu daripada isoproses, namun, ia memainkan peranan penting bukan sahaja dalam pelbagai proses teknologi, tetapi juga dalam alam semula jadi. Dalam artikel ini, kita akan mempertimbangkan apakah proses ini, dan juga memberikan persamaan adiabatik untuk gas ideal.
Ringkasnya gas ideal
Gas ideal ialah gas yang tiada interaksi antara zarahnya dan saiznya sama dengan sifar. Secara semula jadi, sudah tentu, tidak ada seratus peratus gas ideal, kerana mereka semua terdiri daripada molekul dan atom saiz, yang sentiasa berinteraksi antara satu sama lain sekurang-kurangnya dengan bantuan daya van der Waals. Namun begitu, model yang diterangkan selalunya dilakukan dengan ketepatan yang mencukupi untuk menyelesaikan masalah praktikal bagi banyak gas sebenar.
Persamaan utama gas ideal ialah hukum Clapeyron-Mendeleev. Ia ditulis dalam bentuk berikut:
PV=nRT.
Persamaan ini mewujudkan perkadaran langsung antara produktekanan P pada isipadu V dan jumlah bahan n pada suhu mutlak T. Nilai R ialah pemalar gas, yang memainkan peranan sebagai faktor perkadaran.
Apakah itu proses adiabatik?
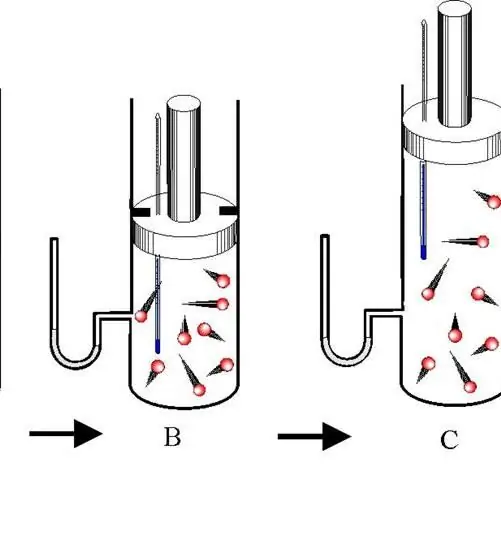
Proses adiabatik ialah peralihan antara keadaan sistem gas di mana tiada pertukaran tenaga dengan persekitaran. Dalam kes ini, ketiga-tiga ciri termodinamik sistem (P, V, T) berubah dan jumlah bahan n kekal malar.
Bezakan antara pengembangan dan pengecutan adiabatik. Kedua-dua proses berlaku hanya disebabkan oleh tenaga dalaman sistem. Jadi, akibat pengembangan, tekanan dan terutamanya suhu sistem menurun secara mendadak. Sebaliknya, pemampatan adiabatik menghasilkan lonjakan positif dalam suhu dan tekanan.
Untuk mengelakkan pertukaran haba antara persekitaran dan sistem, yang kedua mesti mempunyai dinding penebat haba. Di samping itu, memendekkan masa proses dengan ketara mengurangkan aliran haba ke dan dari sistem.
Persamaan Poisson untuk proses adiabatik

Hukum pertama termodinamik ditulis seperti berikut:
Q=ΔU + A.
Dengan kata lain, haba Q yang disampaikan kepada sistem digunakan untuk melaksanakan kerja A oleh sistem dan untuk meningkatkan tenaga dalamannya ΔU. Untuk menulis persamaan adiabatik, seseorang harus meletakkan Q=0, yang sepadan dengan definisi proses yang dikaji. Kami mendapat:
ΔU=-A.
Dengan isochorikproses dalam gas ideal, semua haba pergi untuk meningkatkan tenaga dalaman. Fakta ini membolehkan kami menulis kesamaan:
ΔU=CVΔT.
Di mana CV ialah kapasiti haba isochorik. Kerja A pula dikira seperti berikut:
A=PdV.
Di mana dV ialah perubahan volum yang kecil.
Selain persamaan Clapeyron-Mendeleev, persamaan berikut berlaku untuk gas ideal:
CP- CV=R.
Di mana CP ialah kapasiti haba isobarik, yang sentiasa lebih besar daripada isokhorik, kerana ia mengambil kira kehilangan gas akibat pengembangan.
Menganalisis persamaan yang ditulis di atas dan menyepadukan ke atas suhu dan isipadu, kita sampai pada persamaan adiabatik berikut:
TVγ-1=const.
Di sini γ ialah indeks adiabatik. Ia sama dengan nisbah kapasiti haba isobaric kepada isochoric. Kesamaan ini dipanggil persamaan Poisson untuk proses adiabatik. Menggunakan undang-undang Clapeyron-Mendeleev, anda boleh menulis dua lagi ungkapan yang serupa, hanya melalui parameter P-T dan P-V:
TPγ/(γ-1)=const;
PVγ=const.
Graf adiabatik boleh diberikan dalam paksi yang berbeza. Di bawahnya ditunjukkan dalam paksi P-V.
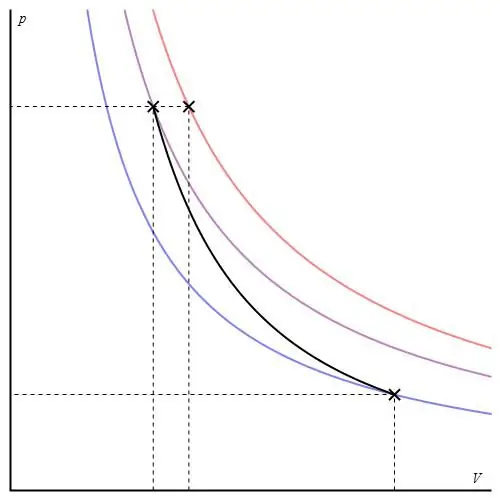
Garis berwarna pada graf sepadan dengan isoterma, lengkung hitam ialah adiabat. Seperti yang dapat dilihat, adiabat berkelakuan lebih tajam daripada mana-mana isoterma. Fakta ini mudah dijelaskan: untuk isoterma, tekanan berubah kembaliberkadar dengan isipadu, tetapi untuk isobath, tekanan berubah lebih cepat, kerana eksponen ialah γ>1 untuk sebarang sistem gas.
Contoh masalah
Secara semula jadi, di kawasan pergunungan, apabila jisim udara bergerak ke atas cerun, tekanannya menurun, ia bertambah dalam jumlah dan menyejuk. Proses adiabatik ini merendahkan takat embun dan menghasilkan kerpasan cecair dan pepejal.

Adalah dicadangkan untuk menyelesaikan masalah berikut: dalam proses mengangkat jisim udara di sepanjang cerun gunung, tekanan menurun sebanyak 30% berbanding tekanan di kaki. Apakah suhunya sama dengan jika di kaki ialah 25 oC?
Untuk menyelesaikan masalah, gunakan persamaan adiabatik berikut:
TPγ/(γ-1)=const.
Adalah lebih baik untuk menulisnya dalam borang ini:
T2/T1=(P2/P 1)(γ-1)/γ.
Jika P1 diambil sebagai 1 atmosfera, maka P2 akan bersamaan dengan 0.7 atmosfera. Untuk udara, indeks adiabatik ialah 1.4, kerana ia boleh dianggap sebagai gas ideal diatomik. Nilai suhu T1 ialah 298.15 K. Menggantikan semua nombor ini ke dalam ungkapan di atas, kita mendapat T2=269.26 K, yang sepadan dengan - 3, 9 oC.






