Salah satu soalan penting dalam kajian sistem termodinamik dalam fizik ialah persoalan sama ada sistem ini boleh melaksanakan beberapa kerja yang berguna. Berkait rapat dengan konsep kerja ialah konsep tenaga dalaman. Dalam artikel ini, kita akan mempertimbangkan apakah tenaga dalaman gas ideal dan memberikan formula untuk mengiranya.
Gas ideal
Mengenai gas, sebagai keadaan terkumpul, yang tidak mempunyai sebarang daya keanjalan di bawah pengaruh luar ke atasnya dan, akibatnya, tidak mengekalkan isipadu dan bentuk, setiap murid sekolah tahu. Konsep gas ideal untuk kebanyakan orang masih tidak dapat difahami dan tidak jelas. Mari kita jelaskan.
Gas ideal ialah sebarang gas yang memenuhi dua syarat penting berikut:
- Zarah yang membentuknya tidak mempunyai saiz. Mereka memang mempunyai saiz, tetapi ia sangat kecil berbanding dengan jarak antara mereka sehingga boleh diabaikan dalam semua pengiraan matematik.
- Zarah tidak berinteraksi antara satu sama lain menggunakan daya atau daya van der Waalssifat lain. Malah, dalam semua gas sebenar, interaksi sedemikian wujud, tetapi tenaganya boleh diabaikan berbanding dengan tenaga purata zarah kinetik.
Keadaan yang diterangkan dipenuhi oleh hampir semua gas sebenar, yang suhunya melebihi 300 K, dan tekanan tidak melebihi satu atmosfera. Untuk tekanan yang terlalu tinggi dan suhu rendah perhatikan sisihan gas daripada kelakuan yang ideal. Dalam kes ini, seseorang bercakap tentang gas sebenar. Ia diterangkan oleh persamaan van der Waals.
Konsep tenaga dalaman gas ideal
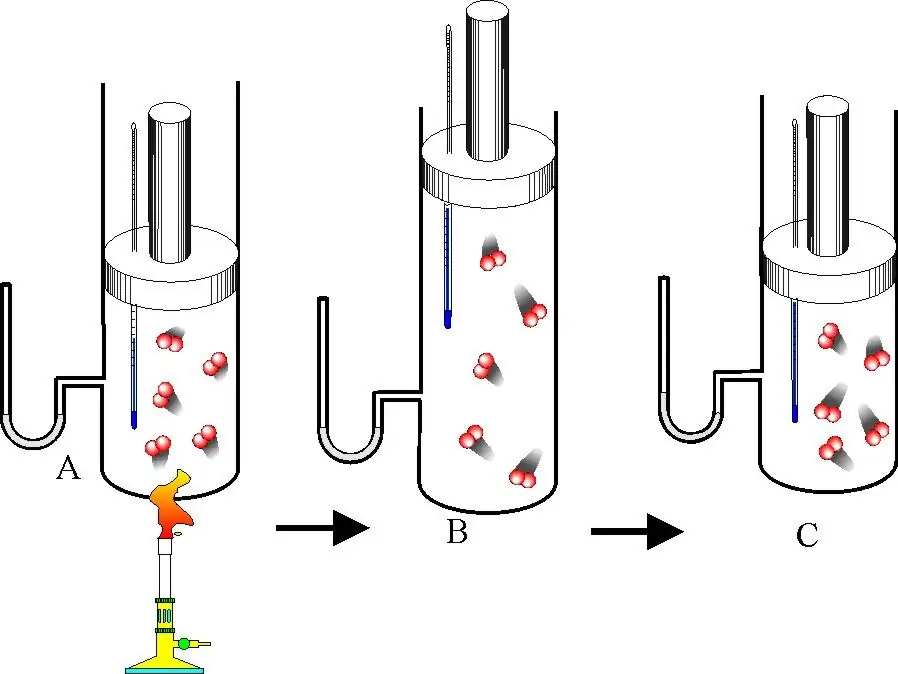
Selaras dengan definisi, tenaga dalaman sistem ialah jumlah tenaga kinetik dan potensi yang terkandung dalam sistem ini. Jika konsep ini digunakan pada gas ideal, maka komponen berpotensi harus dibuang. Sesungguhnya, oleh kerana zarah-zarah gas ideal tidak berinteraksi antara satu sama lain, ia boleh dianggap sebagai bergerak bebas dalam vakum mutlak. Untuk mengekstrak satu zarah daripada sistem yang sedang dikaji, anda tidak perlu melakukan kerja menentang kuasa dalaman interaksi, kerana daya ini tidak wujud.
Oleh itu, tenaga dalaman gas ideal sentiasa bertepatan dengan tenaga kinetiknya. Yang terakhir, seterusnya, ditentukan secara unik oleh jisim molar zarah sistem, bilangannya, serta kelajuan purata gerakan translasi dan putaran. Kelajuan pergerakan bergantung pada suhu. Peningkatan suhu membawa kepada peningkatan tenaga dalaman, begitu juga sebaliknya.
Formula untuktenaga dalaman
Nyatakan tenaga dalaman sistem gas ideal dengan huruf U. Menurut termodinamik, ia ditakrifkan sebagai perbezaan antara entalpi H sistem dan hasil darab tekanan dan isipadu, iaitu:
U=H - pV.
Dalam perenggan di atas, kami mendapati bahawa nilai U sepadan dengan jumlah tenaga kinetik Ekdaripada semua zarah gas:
U=Ek.
Daripada mekanik statistik, dalam rangka teori kinetik molekul (MKT) bagi gas ideal, ia berikutan bahawa tenaga kinetik purata bagi satu zarah Ek1 sama dengan nilai berikut:
Ek1=z/2kBT.
Di sini kB dan T - pemalar dan suhu Boltzmann, z - bilangan darjah kebebasan. Jumlah tenaga kinetik sistem Ek boleh diperolehi dengan mendarab Ek1 dengan bilangan zarah N dalam sistem:
Ek=NEk1=z/2NkBT.
Oleh itu, kami telah memperoleh formula untuk tenaga dalaman gas ideal, ditulis dalam bentuk umum dari segi suhu mutlak dan bilangan zarah dalam sistem tertutup:
U=z/2NkBT.
Gas monoatomik dan poliatomik
Formula untuk U yang ditulis dalam perenggan sebelumnya artikel menyusahkan untuk kegunaan praktikalnya, kerana sukar untuk menentukan bilangan zarah N. Walau bagaimanapun, jika kita mengambil kira takrifan jumlah bahan n, maka ungkapan ini boleh ditulis semula dalam bentuk yang lebih mudah:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Bilangan darjah kebebasan z bergantung pada geometri zarah yang membentuk gas. Oleh itu, untuk gas monoatomik, z=3, kerana atom boleh bergerak bebas hanya dalam tiga arah ruang. Jika gas adalah diatomik, maka z=5, kerana dua lagi darjah kebebasan putaran ditambah kepada tiga darjah kebebasan translasi. Akhir sekali, untuk mana-mana gas poliatomik lain, z=6 (3 translasi dan 3 darjah kebebasan putaran). Dengan mengambil kira perkara ini, kita boleh menulis dalam bentuk berikut formula untuk tenaga dalaman bagi gas ideal monoatomik, diatomik dan poliatomik:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Contoh tugas untuk menentukan tenaga dalaman
Silinder 100 liter mengandungi hidrogen tulen pada tekanan 3 atmosfera. Dengan mengandaikan hidrogen sebagai gas ideal dalam keadaan tertentu, adalah perlu untuk menentukan apakah tenaga dalamannya.

Rumus di atas untuk U mengandungi jumlah bahan dan suhu gas. Dalam keadaan masalah, sama sekali tidak ada yang dikatakan tentang kuantiti ini. Untuk menyelesaikan masalah, perlu mengingati persamaan Clapeyron-Mendeleev universal. Ia mempunyai rupa yang ditunjukkan dalam rajah.
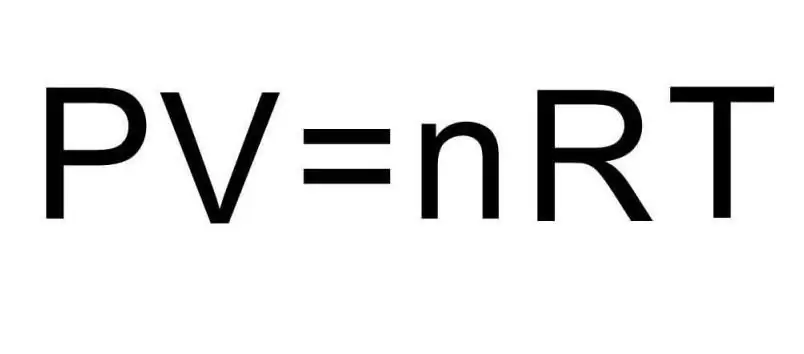
Memandangkan hidrogen H2 ialah molekul diatomik, formula untuk tenaga dalaman ialah:
UH2=5/2nRT.
Membandingkan kedua-dua ungkapan, kami sampai pada formula akhir untuk menyelesaikan masalah:
UH2=5/2PV.
Ia kekal untuk menukar unit tekanan dan isipadu daripada keadaan kepada sistem unit SI, gantikan nilai yang sepadan dalam formula untuk UH2dan dapatkan jawapan: UH2 ≈ 76 kJ.






