Setiap orang semasa hidupnya bertemu dengan jasad yang berada dalam salah satu daripada tiga keadaan jirim agregat. Keadaan pengagregatan yang paling mudah untuk dikaji ialah gas. Dalam artikel itu, kami akan mempertimbangkan konsep gas ideal, memberikan persamaan keadaan sistem, dan juga memberi sedikit perhatian kepada perihalan suhu mutlak.
Keadaan jirim gas
Setiap pelajar mempunyai idea yang baik tentang keadaan jirim yang mereka bincangkan apabila mereka mendengar perkataan "gas". Perkataan ini difahami sebagai badan yang mampu menduduki sebarang isipadu yang disediakan kepadanya. Ia tidak dapat mengekalkan bentuknya, kerana ia tidak dapat menahan walaupun pengaruh luaran yang sedikit. Selain itu, gas tidak mengekalkan isipadu, yang membezakannya bukan sahaja daripada pepejal, tetapi juga daripada cecair.
Seperti cecair, gas ialah bahan cecair. Dalam proses pergerakan jasad pepejal dalam gas, yang terakhir menghalang gerakan ini. Daya yang terhasil dipanggil rintangan. Nilainya bergantung kepadahalaju badan dalam gas.
Contoh gas yang kukuh ialah udara, gas asli yang digunakan untuk memanaskan rumah dan memasak, gas lengai (Ne, Ar) digunakan untuk mengisi tiub cahaya pengiklanan atau digunakan untuk mencipta persekitaran lengai (tidak agresif, pelindung) semasa mengimpal.
Gas ideal
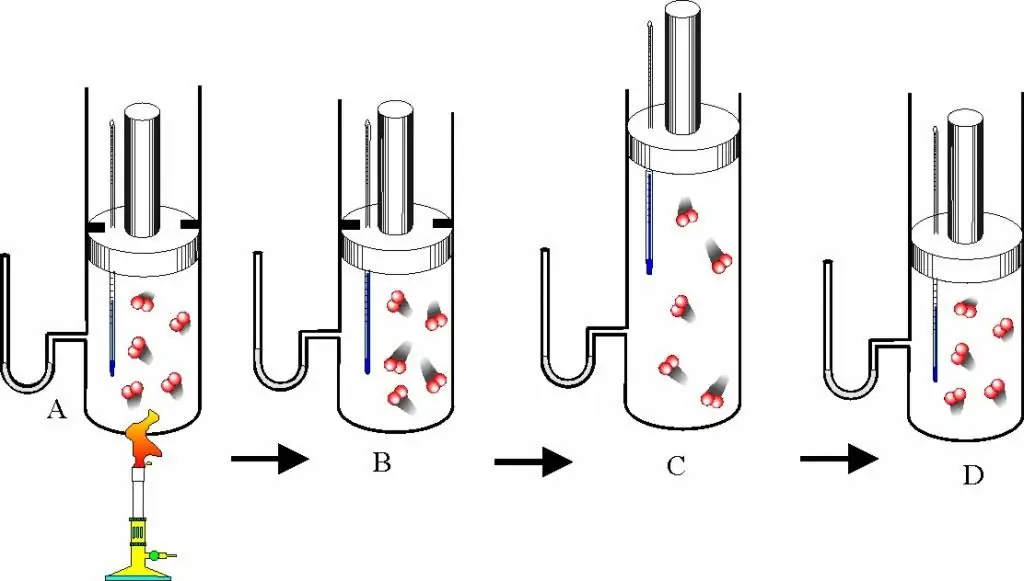
Sebelum meneruskan huraian undang-undang gas dan persamaan keadaan, anda harus memahami dengan baik persoalan tentang apa itu gas ideal. Konsep ini diperkenalkan dalam teori kinetik molekul (MKT). Gas ideal ialah sebarang gas yang memenuhi ciri berikut:
- Zarah yang membentuknya tidak berinteraksi antara satu sama lain kecuali perlanggaran mekanikal langsung.
- Akibat daripada perlanggaran zarah dengan dinding kapal atau antara mereka, tenaga kinetik dan momentumnya dikekalkan, iaitu, perlanggaran itu dianggap benar-benar elastik.
- Zarah tidak mempunyai dimensi, tetapi mempunyai jisim terhingga, iaitu, ia serupa dengan titik material.
Adalah lumrah bahawa sebarang gas tidak ideal, tetapi nyata. Namun begitu, untuk menyelesaikan banyak masalah praktikal, anggaran ini agak sah dan boleh digunakan. Terdapat peraturan empirikal umum yang mengatakan: tanpa mengira sifat kimia, jika gas mempunyai suhu di atas suhu bilik dan tekanan mengikut susunan atmosfera atau lebih rendah, maka ia boleh dianggap ideal dengan ketepatan yang tinggi dan boleh digunakan untuk menggambarkan ia.formula persamaan gas ideal keadaan.
undang-undang Clapeyron-Mendeleev
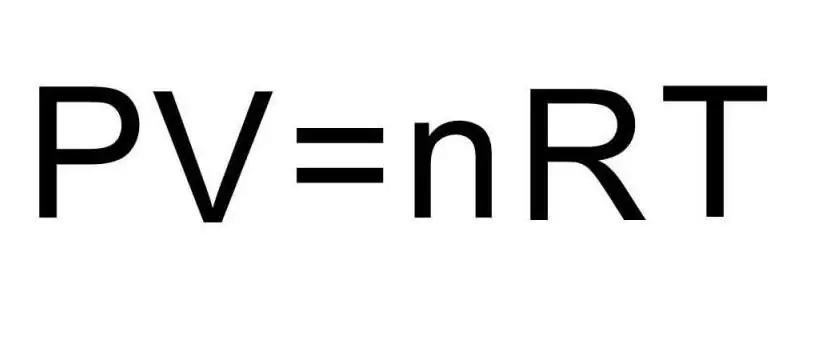
Peralihan antara keadaan agregat jirim yang berbeza dan proses dalam keadaan agregat tunggal dikendalikan oleh termodinamik. Tekanan, suhu dan isipadu ialah tiga kuantiti yang secara unik mentakrifkan mana-mana keadaan sistem termodinamik. Formula untuk persamaan keadaan gas ideal menggabungkan ketiga-tiga kuantiti ini menjadi satu kesamaan. Mari tulis formula ini:
PV=nRT
Di sini P, V, T - masing-masing tekanan, isipadu, suhu. Nilai n ialah jumlah bahan dalam mol, dan simbol R menandakan pemalar sejagat bagi gas. Kesamaan ini menunjukkan bahawa lebih besar hasil darab tekanan dan isipadu, lebih besar mesti hasil darab jumlah bahan dan suhu.

Formula bagi persamaan keadaan gas dipanggil hukum Clapeyron-Mendeleev. Pada tahun 1834, saintis Perancis Emile Clapeyron, meringkaskan hasil eksperimen pendahulunya, datang ke persamaan ini. Walau bagaimanapun, Clapeyron menggunakan beberapa pemalar, yang kemudiannya digantikan oleh Mendeleev dengan satu - pemalar gas sejagat R (8, 314 J / (molK)). Oleh itu, dalam fizik moden, persamaan ini dinamakan sempena nama saintis Perancis dan Rusia.

Borang Persamaan Lain
Di atas, kami menulis persamaan keadaan Mendeleev-Clapeyron bagi gas ideal dalam keadaan yang diterima umum danbentuk yang selesa. Walau bagaimanapun, dalam masalah dalam termodinamik, bentuk yang sedikit berbeza mungkin sering diperlukan. Tiga lagi formula ditulis di bawah, yang mengikuti terus dari persamaan bertulis:
PV=NkBT;
PV=m/MRT;
P=ρRT/M.
Tiga persamaan ini juga universal untuk gas ideal, hanya di dalamnya kuantiti seperti jisim m, jisim molar M, ketumpatan ρ dan bilangan zarah N yang membentuk sistem muncul. Simbol kB di sini menandakan pemalar Boltzmann (1, 3810-23J/K).
Boyle-Mariotte Law
Apabila Clapeyron merangka persamaannya, dia berdasarkan undang-undang gas yang telah ditemui secara eksperimen beberapa dekad sebelumnya. Salah satunya ialah undang-undang Boyle-Mariotte. Ia mencerminkan proses isoterma dalam sistem tertutup, akibatnya parameter makroskopik seperti tekanan dan volum berubah. Jika kita meletakkan T dan n pemalar dalam persamaan keadaan untuk gas ideal, maka hukum gas kemudiannya akan mengambil bentuk:
P1V1=P2V 2
Ini ialah undang-undang Boyle-Mariotte, yang mengatakan bahawa hasil darab tekanan dan isipadu dikekalkan semasa proses isoterma sewenang-wenangnya. Dalam kes ini, nilai P dan V itu sendiri berubah.
Jika anda memplot P(V) atau V(P), maka isoterma akan menjadi hiperbola.
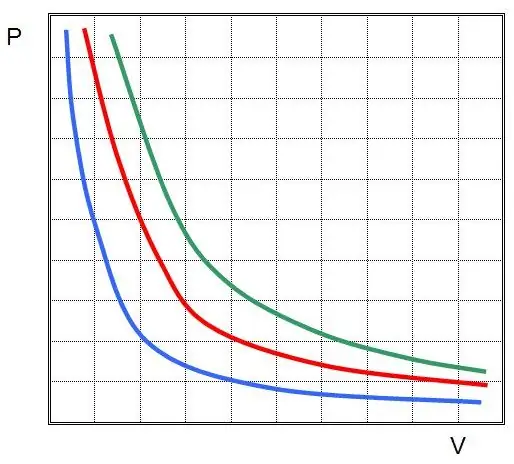
undang-undang Charles dan Gay-Lussac
Undang-undang ini secara matematik menerangkan isobaric dan isochoricproses, iaitu, peralihan sedemikian antara keadaan sistem gas, di mana tekanan dan isipadu dipelihara, masing-masing. Undang-undang Charles boleh ditulis secara matematik seperti berikut:
V/T=const apabila n, P=const.
Undang-undang Gay-Lussac ditulis seperti berikut:
P/T=const apabila n, V=const.
Jika kedua-dua kesamaan dibentangkan dalam bentuk graf, maka kita akan mendapat garis lurus yang condong pada beberapa sudut kepada paksi-x. Graf jenis ini menunjukkan perkadaran langsung antara isipadu dan suhu pada tekanan malar dan antara tekanan dan suhu pada isipadu malar.
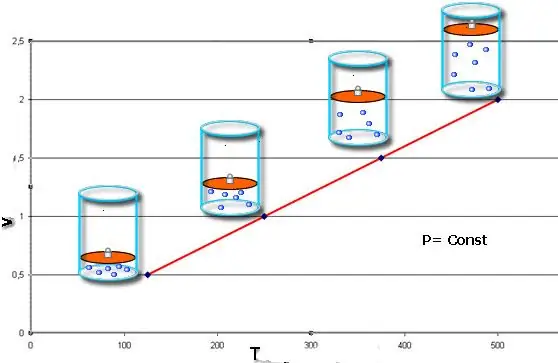
Perhatikan bahawa ketiga-tiga undang-undang gas yang dipertimbangkan tidak mengambil kira komposisi kimia gas, serta perubahan dalam jumlah jirimnya.
Suhu mutlak
Dalam kehidupan seharian, kita sudah biasa menggunakan skala suhu Celsius, kerana ia mudah untuk menerangkan proses di sekeliling kita. Jadi, air mendidih pada 100 oC dan membeku pada 0 oC. Dalam fizik, skala ini ternyata menyusahkan, oleh itu, skala suhu mutlak yang dipanggil, yang diperkenalkan oleh Lord Kelvin pada pertengahan abad ke-19, digunakan. Selaras dengan skala ini, suhu diukur dalam Kelvin (K).
Adalah dipercayai bahawa pada suhu -273, 15 oC tiada getaran haba atom dan molekul, pergerakan ke hadapannya berhenti sepenuhnya. Suhu dalam darjah Celsius ini sepadan dengan sifar mutlak dalam Kelvin (0 K). Daripada definisi inimakna fizikal suhu mutlak berikut: ia ialah ukuran tenaga kinetik zarah yang membentuk jirim, contohnya, atom atau molekul.
Selain maksud fizikal suhu mutlak di atas, terdapat pendekatan lain untuk memahami kuantiti ini. Salah satunya ialah undang-undang gas Charles yang disebutkan. Mari tulis dalam bentuk berikut:
V1/T1=V2/T 2=>
V1/V2=T1/T 2.
Kesamaan terakhir mengatakan bahawa pada jumlah bahan tertentu dalam sistem (contohnya, 1 mol) dan tekanan tertentu (contohnya, 1 Pa), isipadu gas secara unik menentukan suhu mutlak. Dalam erti kata lain, peningkatan dalam isipadu gas dalam keadaan ini hanya mungkin disebabkan oleh peningkatan suhu, dan penurunan dalam isipadu menunjukkan penurunan dalam nilai T.
Ingat bahawa, tidak seperti suhu Celsius, suhu mutlak tidak boleh negatif.
Prinsip Avogadro dan campuran gas
Selain undang-undang gas di atas, persamaan keadaan untuk gas ideal juga membawa kepada prinsip yang ditemui oleh Amedeo Avogadro pada awal abad ke-19, yang menggunakan nama terakhirnya. Prinsip ini menetapkan bahawa isipadu mana-mana gas pada tekanan dan suhu malar ditentukan oleh jumlah bahan dalam sistem. Formula yang sepadan kelihatan seperti ini:
n/V=const apabila P, T=const.
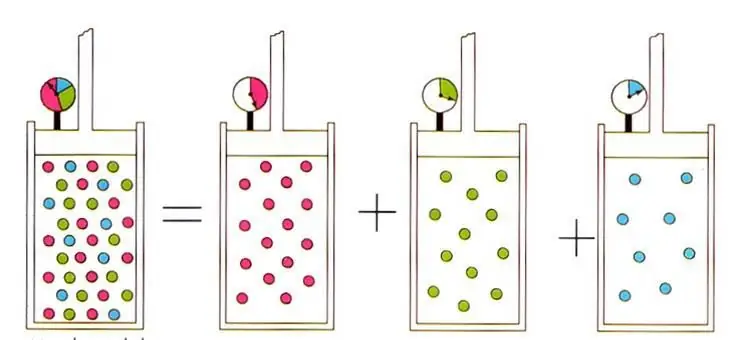
Ungkapan bertulis membawa kepada hukum D alton yang terkenal dalam fizik gas ideal untuk campuran gas. iniundang-undang menyatakan bahawa tekanan separa gas dalam campuran ditentukan secara unik oleh pecahan atomnya.
Contoh penyelesaian masalah
Dalam bekas tertutup dengan dinding tegar yang mengandungi gas ideal, akibat pemanasan, tekanan meningkat sebanyak 3 kali ganda. Adalah perlu untuk menentukan suhu akhir sistem jika nilai awalnya ialah 25 oC.
Pertama, mari tukar suhu daripada darjah Celsius kepada Kelvin, kita ada:
T=25 + 273, 15=298, 15 K.
Memandangkan dinding kapal adalah tegar, proses pemanasan boleh dianggap isochorik. Untuk kes ini, kami menggunakan undang-undang Gay-Lussac, kami mempunyai:
P1/T1=P2/T 2=>
T2=P2/P1T 1.
Oleh itu, suhu akhir ditentukan daripada hasil nisbah tekanan dan suhu awal. Menggantikan data kepada kesamaan, kita mendapat jawapan: T2=894.45 K. Suhu ini sepadan dengan 621.3 oC.






