Pada zaman kita, fizik telah menjadi sains yang sangat biasa. Ia benar-benar hadir di mana-mana. Contoh paling asas: pokok epal tumbuh di halaman anda, dan buah-buahan masak di atasnya, masanya tiba dan epal mula jatuh, tetapi ke arah mana ia jatuh? Terima kasih kepada undang-undang graviti sejagat, janin kita jatuh ke tanah, iaitu, ia turun, tetapi tidak naik. Ia adalah salah satu contoh fizik yang paling terkenal, tetapi mari kita perhatikan termodinamik, atau lebih tepat lagi, kepada keseimbangan fasa, yang tidak kurang pentingnya dalam kehidupan kita.
Termodinamik

Pertama sekali, mari lihat istilah ini. ΘερΜοδυναΜική - beginilah rupa perkataan dalam bahasa Yunani. Bahagian pertama ΘερΜo bermaksud "kehangatan", dan δυναΜική kedua bermaksud "kekuatan". Termodinamik ialah satu cabang fizik yang mengkaji sifat-sifat sistem makroskopik, serta pelbagai cara untuk menukar dan memindahkan tenaga. Dalam bahagian ini, pelbagai keadaan dan proses dikaji khas supaya konsep suhu boleh diperkenalkan ke dalam huraian (ini adalah kuantiti fizik yang mencirikan sistem termodinamik dan diukur menggunakanperalatan tertentu). Semua proses berterusan dalam sistem termodinamik diterangkan hanya dengan kuantiti mikroskopik (tekanan dan suhu, serta kepekatan komponen).
Persamaan Clapeyron-Clausius
Setiap ahli fizik tahu persamaan ini, tetapi mari kita pecahkannya sekeping demi sekeping. Ia merujuk kepada proses keseimbangan peralihan jirim tertentu dari satu fasa ke fasa yang lain. Ini jelas dilihat dalam contoh sedemikian: lebur, penyejatan, pemejalwapan (salah satu cara untuk mengekalkan produk, yang berlaku dengan mengeluarkan sepenuhnya kelembapan). Formula menunjukkan dengan jelas proses yang sedang berjalan:
- n=PV/RT;
- di mana T ialah suhu bahan;
- P-tekanan;
- Haba khusus R bagi peralihan fasa;
- V-perubahan dalam volum tertentu.
Sejarah penciptaan persamaan

Persamaan Clausius-Clapeyron ialah penjelasan matematik yang sangat baik tentang hukum kedua termodinamik. Juga dirujuk sebagai "ketaksamaan Clausius". Sememangnya, teorem itu dibangunkan oleh saintis itu sendiri, yang ingin menjelaskan hubungan antara aliran haba dalam sistem dan entropi, serta persekitarannya. Persamaan ini telah dibangunkan oleh Clausius dalam percubaannya untuk menerangkan dan mengukur entropi. Dalam erti kata literal, teorem memberi kita peluang untuk menentukan sama ada proses kitaran boleh diterbalikkan atau tidak boleh diterbalikkan. Ketaksamaan ini menawarkan kita formula kuantitatif untuk memahami undang-undang kedua.
Saintis itu adalah salah seorang yang pertama mengusahakan idea entropi, malah memberikannyanama proses. Apa yang kini dikenali sebagai teorem Clausius pertama kali diterbitkan pada tahun 1862 dalam karya keenam Rudolf, Mengenai Penggunaan Teorem Kesetaraan Transformasi untuk Kerja Dalaman. Saintis cuba menunjukkan hubungan berkadar antara entropi dan aliran tenaga dengan pemanasan (δ Q) dalam sistem. Dalam pembinaan, tenaga haba ini boleh ditukar menjadi kerja, dan ia boleh diubah menjadi haba melalui proses kitaran. Rudolph membuktikan bahawa "jumlah algebra bagi semua transformasi yang berlaku dalam proses kitaran hanya boleh kurang daripada sifar atau, dalam kes yang melampau, sama dengan sifar."
Sistem terpencil tertutup
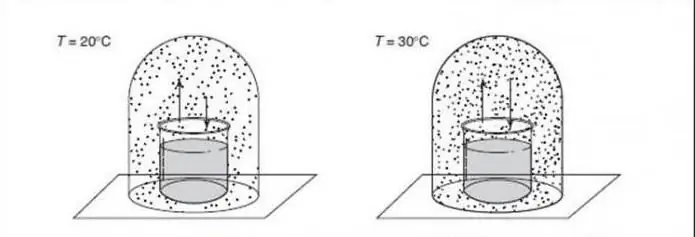
Sistem terpencil ialah salah satu daripada yang berikut:
- Sistem fizikal jauh daripada yang lain yang tidak berinteraksi dengan mereka.
- Sistem termodinamik ditutup oleh dinding tak alih tegar yang tidak boleh dilalui oleh jirim mahupun tenaga.
Walaupun hakikatnya subjek berkaitan secara dalaman dengan gravitinya sendiri, sistem terpencil biasanya diambil melebihi had graviti luaran dan daya jauh yang lain.
Ini boleh dibezakan dengan apa (dalam terminologi yang lebih umum yang digunakan dalam termodinamik) dipanggil sistem tertutup yang dikelilingi oleh dinding terpilih yang melaluinya tenaga boleh dipindahkan dalam bentuk haba atau kerja, tetapi bukan jirim. Dan dengan sistem terbuka di mana jirim dan tenaga masuk atau keluar, walaupun ia mungkin mempunyai pelbagai dinding yang tidak dapat ditembusi dalambahagian sempadannya.
Sistem terpencil mematuhi undang-undang pemuliharaan. Selalunya dalam termodinamik, jirim dan tenaga dianggap sebagai konsep yang berasingan.
Peralihan termodinamik
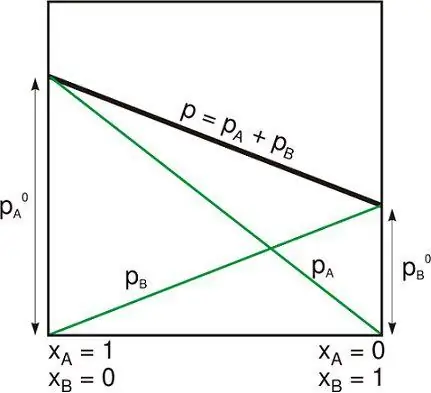
Untuk memahami peralihan fasa kuantum, adalah berguna untuk membandingkannya dengan transformasi klasik (juga dipanggil penyongsangan terma). CPT menerangkan puncak dalam sifat termodinamik sistem. Ia menandakan penyusunan semula zarah. Contoh biasa ialah peralihan beku air, yang menerangkan peralihan lancar antara cecair dan pepejal. Pertumbuhan fasa klasik adalah disebabkan oleh persaingan antara tenaga sistem dan entropi turun naik termanya.
Sistem klasik tidak mempunyai entropi pada suhu sifar dan oleh itu tiada perubahan fasa boleh berlaku. Susunan mereka ditentukan oleh potensi termodinamik terbitan terputus yang pertama. Dan, sudah tentu, ia mempunyai pesanan pertama. Perubahan fasa daripada ferromagnet kepada paramagnet adalah berterusan dan tertib kedua. Perubahan berterusan daripada fasa tertib kepada fasa tidak teratur ini diterangkan oleh parameter tertib yang sifar. Untuk penjelmaan feromagnetik di atas, parameter tertib ialah jumlah kemagnetan sistem.
Potensi Gibbs
Tenaga Bebas Gibbs ialah jumlah maksimum kerja tanpa pengembangan yang boleh dikeluarkan daripada sistem tertutup termodinamik (yang boleh menukar haba dan berfungsi dengan persekitaran). begituhasil maksimum hanya boleh diperolehi dalam proses boleh balik sepenuhnya. Apabila sistem bertukar kembali dari keadaan pertama kepada keadaan kedua, pengurangan tenaga bebas Gibbs adalah sama dengan yang dilakukan oleh sistem dalam persekitarannya, tolak kerja daya tekanan.
Keadaan baki

Keseimbangan termodinamik dan mekanikal ialah konsep aksiomatik termodinamik. Ini ialah keadaan dalaman satu atau lebih sistem yang disambungkan oleh lebih kurang dinding telap atau tidak telap. Dalam keadaan ini, tiada aliran makroskopik tulen jirim atau tenaga, sama ada dalam sistem atau antara sistem.
Dalam konsepnya sendiri tentang keadaan keseimbangan dalaman, perubahan makroskopik tidak berlaku. Sistem secara serentak dalam keseimbangan terma, mekanikal, kimia (malar), sinaran bersama. Mereka mungkin dalam bentuk yang sama. Dalam proses ini, semua paparan disimpan serentak dan selama-lamanya sehingga operasi fizikal rosak. Dalam keseimbangan makroskopik, pertukaran seimbang yang sangat tepat berlaku. Bukti di atas ialah penjelasan fizikal konsep ini.
Asas
Setiap hukum, teorem, formula mempunyai asasnya sendiri. Mari kita lihat 3 asas hukum keseimbangan fasa.
- Fasa ialah satu bentuk jirim, homogen dalam komposisi kimia, keadaan fizikal dan keseimbangan mekanikal. Fasa biasa ialah pepejal, cecair dan gas. Dua cecair tidak larut (atau campuran cecair dengan komposisi berbeza) yang dipisahkan oleh sempadan yang berasingan dianggap sebagai dua fasa yang berbeza dan pepejal tidak boleh larut.
- Bilangan komponen (C) ialah bilangan komponen bebas kimia sistem. Bilangan minimum spesies bebas yang diperlukan untuk menentukan komposisi semua fasa sistem.
- Bilangan darjah kebebasan (F) dalam konteks ini ialah bilangan pembolehubah intensif yang bebas antara satu sama lain.
Pengkelasan mengikut keseimbangan fasa
- Tindak balas pemindahan bersih berterusan (selalunya dipanggil tindak balas keadaan pepejal) berlaku antara bahan pepejal komposisi berbeza. Ia mungkin termasuk unsur-unsur yang terdapat dalam cecair (H, C), tetapi unsur-unsur ini dikekalkan dalam fasa pepejal, jadi tiada fasa cecair terlibat sebagai bahan tindak balas atau produk (H2O, CO2). Tindak balas pemindahan tulen pepejal boleh berterusan atau tidak berterusan, atau terminal.
- Polymorphic ialah sejenis tindak balas fasa pepejal khas yang merangkumi fasa komposisi yang sama. Contoh klasik ialah tindak balas antara aluminium silikat kyanite-sillimanit-andalusit, penukaran grafit kepada berlian pada tekanan tinggi, dan keseimbangan kalsium karbonat.
Hukum keseimbangan

Peraturan Kilang Gibbs telah dicadangkan oleh Josiah Willard Gibbs dalam makalah terkenalnya bertajuk "The Equilibrium of Heterogenous Substances", yang muncul dari 1875 hingga 1878. Ia terpakai kepadasistem heterogen berbilang komponen bukan reaktif dalam keseimbangan termodinamik dan merupakan kesamaan tertentu:
- F=C-P+2;
- di mana F ialah bilangan darjah kebebasan;
- C - bilangan komponen;
- P - bilangan fasa dalam keseimbangan termodinamik antara satu sama lain.
Bilangan darjah kebebasan ialah bilangan pembolehubah intensif yang tidak diduduki. Bilangan terbesar parameter termodinamik, seperti suhu atau tekanan, yang boleh berubah secara serentak dan sewenang-wenangnya tanpa menjejaskan satu sama lain. Contoh sistem satu komponen ialah satu dengan satu bahan kimia tulen, manakala sistem dua komponen, seperti campuran air dan etanol, mempunyai dua komponen bebas. Peralihan fasa biasa (keseimbangan fasa) ialah pepejal, cecair, gas.
Peraturan fasa pada tekanan malar
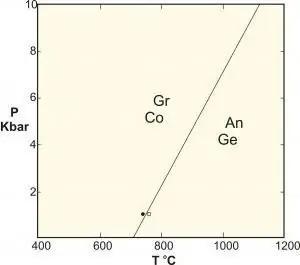
Untuk aplikasi dalam sains bahan yang berurusan dengan perubahan fasa antara struktur pepejal yang berbeza, tekanan malar sering berlaku (cth. satu atmosfera) dan diabaikan sebagai darjah kebebasan, jadi peraturannya menjadi: F=C - P + 1.
Formula ini kadangkala diperkenalkan di bawah nama "peraturan fasa terkondensasi", tetapi seperti yang kita ketahui, ia tidak boleh digunakan untuk sistem ini yang tertakluk kepada tekanan tinggi (contohnya, dalam geologi), kerana akibat daripada ini tekanan boleh menyebabkan akibat bencana.
Nampaknya keseimbangan fasa hanyalah frasa kosong dan terdapat beberapa proses fizikal di mana detik initerlibat, tetapi, seperti yang kita lihat, tanpa itu, banyak undang-undang yang kita tahu tidak berfungsi, jadi anda perlu membiasakan diri dengan peraturan yang unik, berwarna-warni, walaupun sedikit membosankan. Ilmu ini telah membantu ramai orang. Mereka belajar cara menerapkannya pada diri mereka sendiri, sebagai contoh, juruelektrik, mengetahui peraturan untuk bekerja dengan fasa, boleh melindungi diri mereka daripada bahaya yang tidak perlu.






