Keadaan tiga dimensi air cecair sukar untuk dikaji, tetapi banyak yang telah dipelajari dengan menganalisis struktur hablur ais. Empat atom oksigen yang berinteraksi dengan hidrogen bersebelahan menduduki bucu tetrahedron (tetra=empat, hedron=satah). Purata tenaga yang diperlukan untuk memecahkan ikatan sedemikian dalam ais dianggarkan pada 23 kJ/mol-1.

Keupayaan molekul air membentuk bilangan rantai hidrogen tertentu, serta kekuatan tertentu, mencipta takat lebur yang luar biasa tinggi. Apabila ia cair, ia dipegang oleh air cair, yang strukturnya tidak teratur. Kebanyakan ikatan hidrogen terherot. Ia memerlukan sejumlah besar tenaga dalam bentuk haba untuk memecahkan kekisi kristal ais terikat hidrogen.
Ciri-ciri rupa ais (Ih)
Ramai penduduk tertanya-tanya apakah jenis ais kekisi kristal. PerluPerlu diingatkan bahawa ketumpatan kebanyakan bahan meningkat semasa pembekuan, apabila pergerakan molekul perlahan dan kristal padat terbentuk. Ketumpatan air juga meningkat apabila ia menyejuk maksimum pada 4°C (277K). Kemudian, apabila suhu jatuh di bawah nilai ini, ia mengembang.
Peningkatan ini disebabkan oleh pembentukan hablur ais terikat hidrogen terbuka dengan kekisi dan ketumpatan yang lebih rendah, di mana setiap molekul air terikat tegar oleh unsur di atas dan empat nilai lain, sambil bergerak cukup pantas untuk mempunyai lebih banyak jisim. Oleh kerana tindakan ini berlaku, cecair membeku dari atas ke bawah. Ini mempunyai hasil biologi yang penting, akibatnya lapisan ais di kolam melindungi makhluk hidup dari kesejukan yang melampau. Selain itu, dua sifat tambahan air berkaitan dengan ciri hidrogennya: haba tentu dan penyejatan.
Penerangan terperinci tentang struktur
Kriteria pertama ialah jumlah yang diperlukan untuk menaikkan suhu 1 gram bahan sebanyak 1°C. Menaikkan darjah air memerlukan jumlah haba yang agak besar kerana setiap molekul terlibat dalam banyak ikatan hidrogen yang mesti dipecahkan supaya tenaga kinetik meningkat. Ngomong-ngomong, banyaknya H2O dalam sel dan tisu semua organisma multisel yang besar bermakna turun naik suhu di dalam sel diminimumkan. Ciri ini penting, kerana kadar kebanyakan tindak balas biokimiasensitif.
Haba pengewapan air juga jauh lebih tinggi daripada kebanyakan cecair lain. Sebilangan besar haba diperlukan untuk menukar jasad ini menjadi gas, kerana ikatan hidrogen mesti dipecahkan agar molekul air terkehel antara satu sama lain dan memasuki fasa tersebut. Jasad boleh tukar ialah dipol kekal dan boleh berinteraksi dengan sebatian lain yang serupa dan yang terion dan terlarut.
Bahan lain yang dinyatakan di atas boleh bersentuhan hanya jika terdapat kekutuban. Sebatian inilah yang terlibat dalam struktur unsur-unsur ini. Di samping itu, ia boleh menyelaraskan di sekeliling zarah-zarah ini yang terbentuk daripada elektrolit, supaya atom oksigen negatif molekul air berorientasikan kepada kation, dan ion positif dan atom hidrogen berorientasikan kepada anion.
Dalam pepejal, sebagai peraturan, kisi kristal molekul dan yang atom terbentuk. Iaitu, jika iodin dibina sedemikian rupa sehingga ia mengandungi I2, , maka dalam karbon dioksida pepejal, iaitu, dalam ais kering, molekul CO2 adalah terletak di nod kekisi kristal . Apabila berinteraksi dengan bahan yang serupa, ais mempunyai kekisi kristal ionik. Grafit, contohnya, yang mempunyai struktur atom berdasarkan karbon, tidak dapat mengubahnya, sama seperti berlian.
Apa yang berlaku apabila kristal garam meja larut dalam air: molekul polar tertarik kepada unsur bercas dalam kristal, yang membawa kepada pembentukan zarah natrium dan klorida yang serupa pada permukaannya, menghasilkan jasad initerkehel antara satu sama lain, dan ia mula larut. Dari sini dapat diperhatikan bahawa ais mempunyai kekisi kristal dengan ikatan ionik. Setiap Na + terlarut menarik hujung negatif beberapa molekul air, manakala setiap Cl terlarut - menarik hujung positif. Cangkang yang mengelilingi setiap ion dipanggil sfera lepas dan biasanya mengandungi beberapa lapisan zarah pelarut.
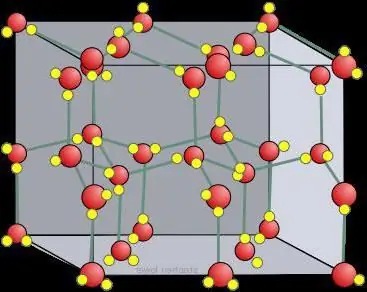
Kekisi kristal ais kering
Pembolehubah atau ion yang dikelilingi oleh unsur dikatakan sulfat. Apabila pelarut adalah air, zarah tersebut terhidrat. Oleh itu, mana-mana molekul polar cenderung untuk dilarutkan oleh unsur-unsur badan cecair. Dalam ais kering, jenis kekisi kristal membentuk ikatan atom dalam keadaan pengagregatan, yang tidak berubah. Perkara lain ialah ais kristal (air beku). Sebatian organik ionik seperti karboksilase dan amina terproton mesti larut dalam kumpulan hidroksil dan karbonil. Zarah-zarah yang terkandung dalam struktur sedemikian bergerak antara molekul, dan sistem kutubnya membentuk ikatan hidrogen dengan jasad ini.
Sudah tentu, bilangan kumpulan terakhir yang ditunjukkan dalam molekul mempengaruhi keterlarutannya, yang juga bergantung pada tindak balas pelbagai struktur dalam unsur: contohnya, alkohol satu, dua dan tiga karbon boleh bercampur. dengan air, tetapi hidrokarbon yang lebih besar dengan sebatian hidroksil tunggal adalah kurang cair dalam cecair.
Heksagonal Ih adalah serupa dengan bentukkekisi kristal atom. Untuk ais dan semua salji semula jadi di Bumi, ia kelihatan betul-betul seperti ini. Ini dibuktikan dengan simetri kekisi kristal ais, yang tumbuh daripada wap air (iaitu, kepingan salji). Ia berada dalam kumpulan angkasa P 63/mm daripada 194; D 6j, kelas Laue 6/mm; serupa dengan β-, yang mempunyai gandaan 6 paksi heliks (putaran mengelilingi sebagai tambahan kepada anjakan di sepanjangnya). Ia mempunyai struktur ketumpatan rendah yang agak terbuka dengan kecekapan rendah (~1/3) berbanding struktur kubik ringkas (~1/2) atau kubik berpusat muka (~3/4).
Berbanding dengan ais biasa, kisi kristal ais kering, yang diikat oleh molekul CO2, adalah statik dan berubah hanya apabila atom mereput.
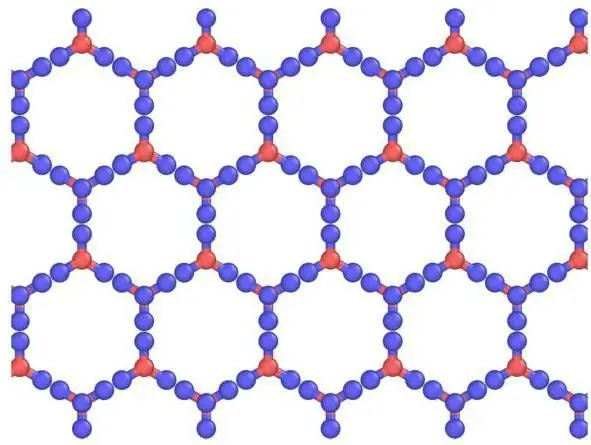
Penerangan tentang jeriji dan unsurnya
Kristal boleh dilihat sebagai model kristal, yang terdiri daripada helaian yang diletakkan satu di atas yang lain. Ikatan hidrogen adalah tersusun, manakala pada hakikatnya ia adalah rawak, kerana proton boleh bergerak di antara molekul air (ais) pada suhu di atas kira-kira 5 K. Sesungguhnya, ada kemungkinan proton berkelakuan seperti cecair kuantum dalam aliran terowong yang berterusan. Ini dipertingkatkan dengan penyerakan neutron, menunjukkan ketumpatan penyebarannya di tengah-tengah antara atom oksigen, menunjukkan penyetempatan dan gerakan bersepadu. Di sini terdapat persamaan ais dengan kisi kristal molekul atom.
Molekul mempunyai susunan rantai hidrogen yang berperingkatberkenaan dengan tiga jirannya di dalam pesawat itu. Unsur keempat mempunyai susunan ikatan hidrogen yang gerhana. Terdapat sedikit sisihan daripada simetri heksagon sempurna, kerana sel unit adalah 0.3% lebih pendek ke arah rantai ini. Semua molekul mengalami persekitaran molekul yang sama. Terdapat ruang yang cukup di dalam setiap "kotak" untuk menampung zarah air celahan. Walaupun tidak dipertimbangkan secara umum, ia baru-baru ini telah dikesan dengan berkesan oleh pembelauan neutron kekisi kristal serbuk ais.
Bahan Berubah
Badan heksagon mempunyai tiga titik dengan air cecair dan gas 0.01 ° C, 612 Pa, unsur pepejal - tiga -21.985 ° C, 209.9 MPa, sebelas dan dua -199.8 ° C, 70 MPa, serta - 34.7 ° C, 212.9 MPa. Pemalar dielektrik ais heksagon ialah 97.5.
Lengkung lebur unsur ini diberikan oleh MPa. Persamaan keadaan tersedia, sebagai tambahan kepada mereka, beberapa ketaksamaan mudah yang mengaitkan perubahan sifat fizik kepada suhu ais heksagon dan ampaian akueusnya. Kekerasan berubah-ubah dengan darjah naik dari atau di bawah gipsum (≦2) pada 0°C kepada feldspar (6 Mohs) pada -80°C, perubahan yang luar biasa besar dalam kekerasan mutlak (> 24 kali).
Kekisi kristal heksagon ais membentuk plat dan lajur heksagon, di mana muka atas dan bawah ialah satah asas {0 0 0 1} dengan entalpi 5.57 μJ cm -2, dan bahagian sisi lain yang setara dipanggil bahagian prisma {1 0 -1 0} dengan 5, 94µJ cm -2. Permukaan sekunder {1 1 -2 0} dengan 6.90 ΜJ ˣ cm -2 boleh dibentuk di sepanjang satah yang dibentuk oleh sisi struktur.
Struktur sedemikian menunjukkan penurunan anomali dalam kekonduksian terma dengan peningkatan tekanan (serta ais padu dan amorfus berketumpatan rendah), tetapi berbeza daripada kebanyakan kristal. Ini disebabkan oleh perubahan dalam ikatan hidrogen, yang mengurangkan kelajuan melintang bunyi dalam kekisi kristal ais dan air.
Terdapat kaedah yang menerangkan cara menyediakan sampel kristal besar dan sebarang permukaan ais yang dikehendaki. Diandaikan bahawa ikatan hidrogen pada permukaan jasad heksagon yang dikaji akan lebih teratur daripada di dalam sistem pukal. Spektroskopi variasi dengan penjanaan frekuensi fasa-kekisi telah menunjukkan bahawa terdapat asimetri struktur antara dua lapisan atas (L1 dan L2) dalam rantaian HO bawah permukaan permukaan basal ais heksagon. Ikatan hidrogen yang diterima pakai pada lapisan atas heksagon (L1 O ··· HO L2) adalah lebih kuat daripada yang diterima dalam lapisan kedua kepada pengumpulan atas (L1 OH ··· O L2). Struktur ais heksagon interaktif tersedia.
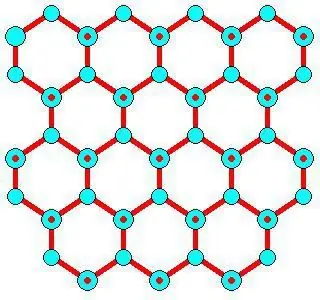
Ciri Pembangunan
Bilangan minimum molekul air yang diperlukan untuk membentuk ais adalah lebih kurang 275 ± 25, manakala bagi gugusan ikosahedral lengkap sebanyak 280. Pembentukan berlaku pada kadar 10 10 pada antara muka air-air dan bukan dalam air pukal. Pertumbuhan hablur ais bergantung pada kadar pertumbuhan yang berbeza dari pelbagaitenaga. Air mesti dilindungi daripada membeku apabila mengawet spesimen biologi, makanan dan organ.
Ini biasanya dicapai dengan kadar penyejukan yang cepat, menggunakan sampel kecil dan cryoconservator, dan meningkatkan tekanan untuk menukleus ais dan mencegah kerosakan sel. Tenaga bebas ais/cecair meningkat daripada ~30 mJ/m2 pada tekanan atmosfera kepada 40 mJ/m-2 pada 200 MPa, menunjukkan sebab kesan ini berlaku.
Apakah jenis kekisi kristal yang bercirikan ais
Sebagai alternatif, ia boleh tumbuh lebih cepat daripada permukaan prisma (S2), pada permukaan tasik yang cepat beku atau bergolak yang terganggu secara rawak. Pertumbuhan daripada muka {1 1 -2 0} adalah sekurang-kurangnya sama, tetapi mengubahnya menjadi tapak prisma. Data mengenai pembangunan kristal ais telah disiasat sepenuhnya. Kadar pertumbuhan relatif unsur-unsur muka yang berbeza bergantung pada keupayaan untuk membentuk tahap penghidratan sendi yang besar. Suhu (rendah) air di sekeliling menentukan tahap percabangan dalam hablur ais. Pertumbuhan zarah dihadkan oleh kadar resapan pada tahap penyejukan super yang rendah, iaitu <2 ° C, menghasilkan lebih banyak daripadanya.

Tetapi dihadkan oleh kinetik pembangunan pada tahap kemurungan yang lebih tinggi iaitu >4°C, mengakibatkan pertumbuhan jarum. Bentuk ini serupa dengan struktur ais kering (mempunyai kekisi kristal dengan struktur heksagon), pelbagaiciri-ciri perkembangan permukaan dan suhu air di sekeliling (supersejuk), yang berada di belakang bentuk rata kepingan salji.
Pembentukan ais di atmosfera sangat mempengaruhi pembentukan dan sifat awan. Feldspar, yang terdapat dalam habuk padang pasir yang memasuki atmosfera dalam berjuta-juta tan setahun, adalah pembentuk penting. Simulasi komputer telah menunjukkan bahawa ini disebabkan oleh nukleasi satah kristal ais prisma pada satah permukaan tenaga tinggi.
Beberapa elemen dan kekisi lain
Bahan terlarut (kecuali helium dan hidrogen yang sangat kecil, yang boleh memasuki celahan) tidak boleh dimasukkan ke dalam struktur Ih pada tekanan atmosfera, tetapi dipaksa keluar ke permukaan atau lapisan amorf di antara zarah-zarah badan mikrokristalin. Terdapat beberapa unsur lain di tapak kekisi ais kering: ion chaotropic seperti NH4 + dan Cl - yang termasuk dalam pembekuan cecair yang lebih ringan daripada cecair kosmotropik lain seperti Na + dan SO42-, jadi mengalihkannya tidak dapat dilakukan kerana fakta bahawa ia membentuk lapisan nipis cecair yang tinggal di antara kristal. Ini boleh menyebabkan pengecasan elektrik pada permukaan disebabkan oleh pemisahan air permukaan yang mengimbangi cas yang tinggal (yang juga boleh membawa kepada sinaran magnet) dan perubahan dalam pH filem cecair sisa, cth. NH 42SO4 menjadi lebih berasid dan NaCl menjadi lebih asas.
Ia berserenjang dengan mukakekisi kristal ais menunjukkan lapisan seterusnya melekat (dengan atom O berwarna hitam). Ia dicirikan oleh permukaan basal yang tumbuh perlahan {0 0 0 1}, di mana hanya molekul air terpencil yang melekat. Permukaan prisma {1 0 -1 0} yang berkembang pesat di mana sepasang zarah yang baru melekat boleh terikat antara satu sama lain dengan hidrogen (satu ikatan hidrogen/dua molekul unsur). Muka yang paling cepat tumbuh ialah {1 1 -2 0} (prismatik sekunder), di mana rantai zarah yang baru melekat boleh berinteraksi antara satu sama lain melalui ikatan hidrogen. Salah satu rantai/molekul unsurnya ialah bentuk yang membentuk rabung yang membahagi dan menggalakkan perubahan menjadi dua sisi prisma.
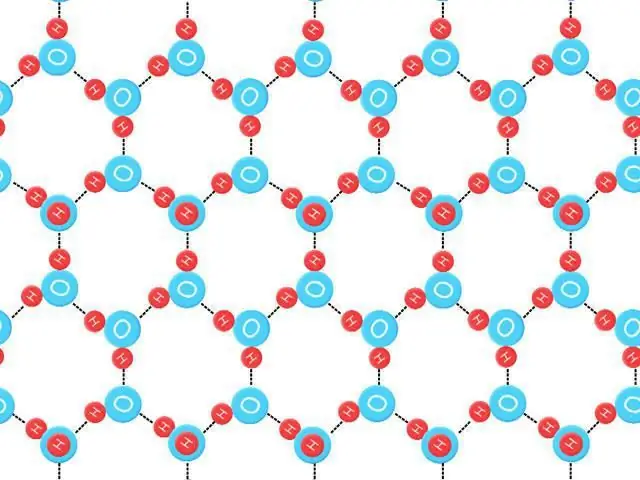
Entropi titik sifar
Boleh ditakrifkan sebagai S 0=k B ˣ Ln (N E0), dengan k B ialah pemalar Boltzmann, NE ialah bilangan konfigurasi pada tenaga E, dan E0 ialah tenaga terendah. Nilai untuk entropi ais heksagon pada sifar Kelvin ini tidak melanggar undang-undang ketiga termodinamik "Entropi kristal ideal pada sifar mutlak adalah betul-betul sifar", kerana unsur dan zarah ini tidak ideal, mempunyai ikatan hidrogen yang tidak teratur.
Dalam badan ini, ikatan hidrogen adalah rawak dan cepat berubah. Struktur ini tidak betul-betul sama dalam tenaga, tetapi memanjangkan kepada sebilangan besar keadaan rapat yang bertenaga, mematuhi "peraturan ais". Entropi titik sifar ialah gangguan yang akan kekal walaupun bahan itu boleh disejukkan kepada mutlaksifar (0 K=-273, 15 ° C). Menghasilkan kekeliruan percubaan untuk ais heksagon 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Secara teorinya, adalah mungkin untuk mengira sifar entropi hablur ais yang diketahui dengan ketepatan yang lebih besar (mengabaikan kecacatan dan penyebaran tahap tenaga) daripada menentukannya secara eksperimen.
Saintis dan kerja mereka dalam bidang ini
Boleh ditakrifkan sebagai S 0=k B ˣ Ln (N E0), dengan k B ialah pemalar Boltzmann, NE ialah bilangan konfigurasi pada tenaga E, dan E0 ialah tenaga terendah. Nilai untuk entropi ais heksagon pada sifar Kelvin ini tidak melanggar undang-undang ketiga termodinamik "Entropi kristal ideal pada sifar mutlak adalah betul-betul sifar", kerana unsur dan zarah ini tidak ideal, mempunyai ikatan hidrogen yang tidak teratur.
Dalam badan ini, ikatan hidrogen adalah rawak dan cepat berubah. Struktur ini tidak betul-betul sama dalam tenaga, tetapi memanjangkan kepada sebilangan besar keadaan rapat yang bertenaga, mematuhi "peraturan ais". Entropi titik sifar ialah gangguan yang akan kekal walaupun bahan boleh disejukkan kepada sifar mutlak (0 K=-273.15°C). Menghasilkan kekeliruan percubaan untuk ais heksagon 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Secara teorinya, adalah mungkin untuk mengira sifar entropi hablur ais yang diketahui dengan ketepatan yang lebih besar (mengabaikan kecacatan dan penyebaran tahap tenaga) daripada menentukannya secara eksperimen.

Walaupun susunan proton dalam ais pukal tidak tersusun, permukaan mungkin lebih suka susunan zarah ini dalam bentuk jalur gantung atom H dan pasangan O-tunggal (entropi sifar dengan ikatan hidrogen tersusun). Gangguan titik sifar ZPE, J ˣ mol -1 ˣ K -1 dan lain-lain ditemui. Daripada semua perkara di atas, adalah jelas dan boleh difahami jenis kekisi kristal yang menjadi ciri ais.






